Pengaruh penambahan konsentrasi CMC-Na sebagai gelling agent pada sediaan sunscreen gel ekstrak temugiring (Curcuma heyneana Val.) terhadap sifat fisik dan stabilitas sediaan dengan propilen glikol sebagai humectant - USD Repository
Teks penuh
Gambar
Dokumen terkait
Penelitian tentang optimasi formula gel sunscreen ekstrak etanol rimpang kunir putih (Curcuma mangga Val.) dengan sorbitol dan propilen glikol sebagai humectant telah
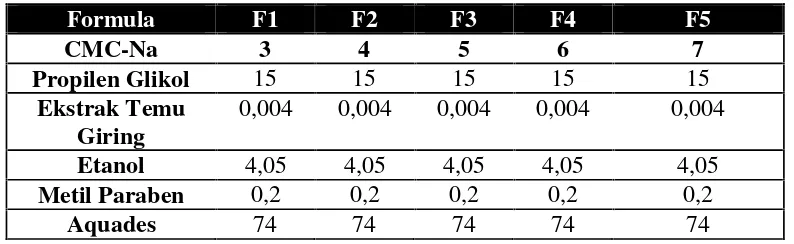
Penelitian ini bertujuan untuk menentukan perbandingan jumlah gelling agent CMC Na dan humektan propilen glikol, menentukan faktor yang dominan pada gel
Tujuan penelitian ini adalah untuk menentukan komposisi optimum dari CMC-Na dan gliserin serta mengetahui faktor mana yang dominan dalam menghasilkan sediaan gel yang
Penelitian ini bertujuan untuk mengetahui pengaruh konsentrasi CMC-Na ( gelling agent) dan propilen glikol (humektan) terhadap sifat fisik dan stabilitas fisik gel
PENGARUH KONSENTRASI CMC-NA SEBAGAI GELLING AGENT TERHADAP SIFAT FISIK DAN STABILITAS SEDIAAN GEL HAND SANITIZER MINYAK ATSIRI DAUN MINT (Oleum Mentha piperita
carbomer dan humektan gliserin serta untuk mengetahui faktor (carbomer, gliserin, dan interaksi carbomer dan gliserin) yang dominan dalam menghasilkan sediaan gel
Sejauh penelusuran pustaka yang dilakukan penulis, penelitian tentang optimasi formula gel sunscreen ekstrak etanol rimpang kunir putih ( Curcuma mangga Val.): tinjauan
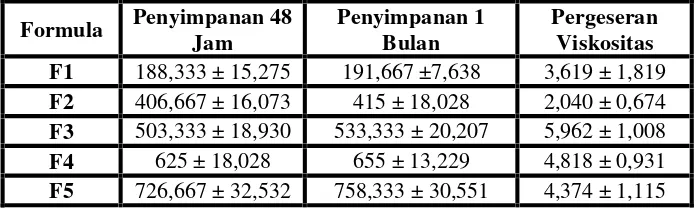
Level yang digunakan pada rancangan optimasi menggunakan CCD tidak memberikan model yang signifikan sehingga area optimum faktor CMC-Na dan propilen glikol sediaan