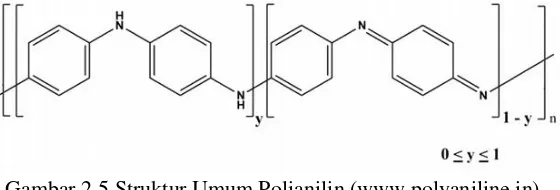
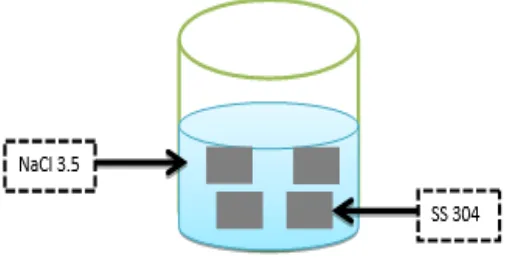
ANALISA LAJU KOROSI PADA BAJA SS304 DENGAN VARIASI MATERIAL PELAPIS PADA LINGKUNGAN SALINITAS TINGGI NaCl 3,5 M
Teks penuh
Gambar

Dokumen terkait
Buah merah memiliki kemampuan yang lebih baik dibandingkan dengan obat standar (hepasil) dalam mencegah terjadinya kerusakan sel hati dengan ditunjukkan menurunnya
Rupture Anterior Cruciate Ligamen ialah robeknya ligamen sendi lutut yang bisa disebabkan karena adanya trauma, baik trauma langsung seperti adanya benturan langsung pada lutut
VII, 66 : Mengenai penghargaan dan penghormatan, Sariputta berkata bahwa hal-hal ini berguna dalam melenyapkan apa yang tidak baik dan mengembangkan apa yang baik: penghargaan
Dengan menggunakan penilaian yang didasarkan pada Peraturan Menteri Pe- kerjaan Umum No 32/PRT/M/2007 tentang Pedoman Operasi dan Pemeli- haraan Jaringan Irigasi, dari
Barang siapa dengan sengaja menjalankan sebagai alat pembayaran yang sah mata uang atau uang kertas yang dari pihak Pemerintah tidak diakui sebagai alat
Pipet 5 ml hasil saringan dan masukkan dalam tabung reaksi, tambahkan 20 ml aquadest dan reagen B sebanyak 8 ml, didiamkan selama 20 menit selanjutnya tetapkan absorban
Suhu air merupakan salah satu faktor lingkungan yang berpengaruh pada perkembangan larva kepiting bakau. Tujuan penelitian adalah untuk mengetahui pengaruh perbedaan suhu air
Laju alir distilat berpengaruh terhadap kecepatan air bergerak turun di silinder luar separator relatif terhadap kecepatan minyak nilam bergerak naik dalam air yang