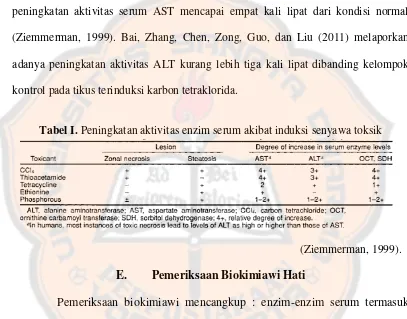
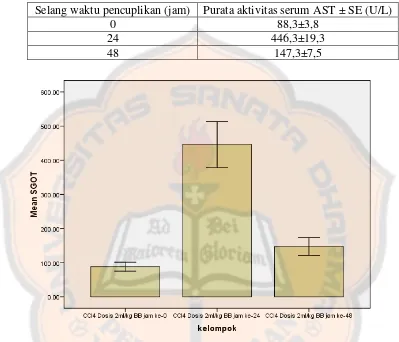
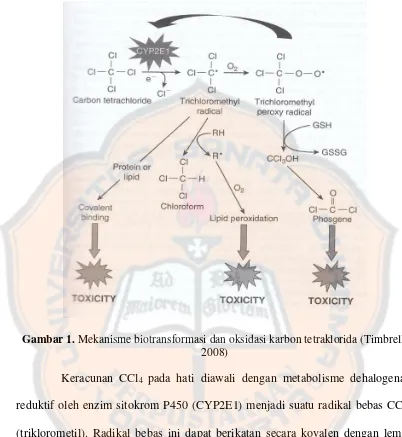
Efek hepatoprotektif jangka panjang ekstrak metanol-air biji persea americana mill. terhadap aktivitas alt-ast serum pada tikus jantan wistar terinduksi karbon tetraklorida - USD Repository
Teks penuh
Gambar



Garis besar
Dokumen terkait
diLlnpks ud Fehi $ttulsyr
Penelitian ini bertujuan untuk mengetahui proses pembuatan indikator asam basa dari kulit buah kesumba ( Bixa orellana L.), mengetahui perubahan warna yang ditimbulkan oleh
Toksisitas akut Berdasarkan data yang tersedia, kriteria klasifikasi tidak terpenuhi.. Korosi kulit/iritasi Menyebabkan
menggunakn bahan/barang yang ditemukan di lingkungan tempat tinggal siswa. Melihat penjelasan di atas dapat disimpulkan bahwa KIT IPA merupakan alat yang berguna
nkumn kon.jstensi penycl€nggara nega.a terh.dap prinsip kedaulabn Bkyat dalam UUD 1945. Paso perubahan UoD 1945, sisten pemilihan udun anggota legislatif setalu
TtrRTUMBUTLA.N DAN PRODUKSI RUM}M BXNGGAL{. (P@1
6 dan histamine yang mengakibatkan terjadinya disfungsi sel endotel dan terjadi kebocoran plasma. Peningkatan C3a dan C5a terjadi melalui aktivasi oleh kompleks virus-antibodi
Maka, perlu disiapkan sumber daya yang berkualitas dan unggul untuk memenuhi kebutuhan yang meningkat untuk produktivitas yang lebih baik dan tanggung jawab sosial yang tinggi..