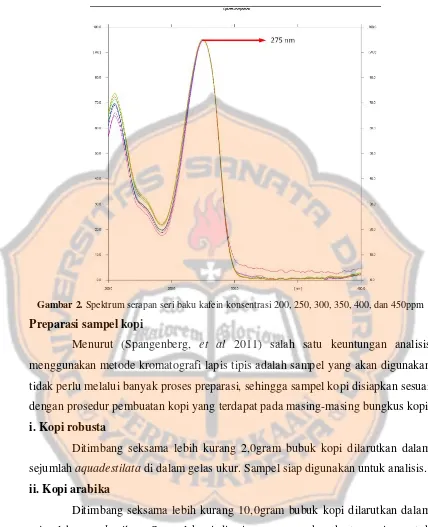
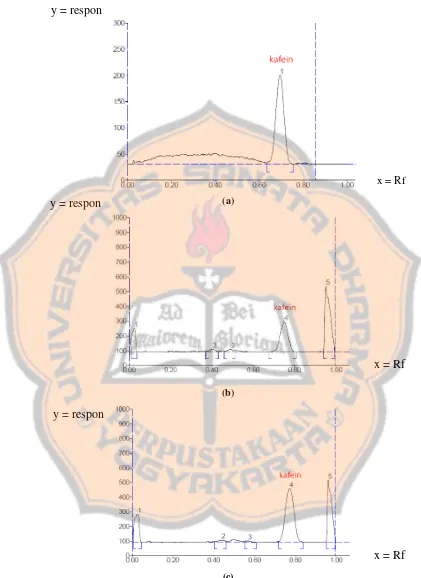
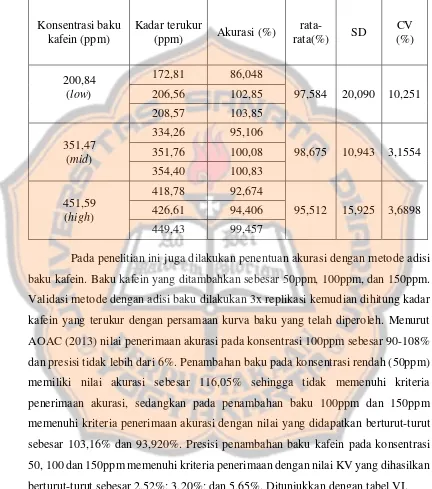
VALIDASI METODE THIN-LAYER CHROMATOGRAPHY (TLC)- DENSITOMETRI PADA PENETAPAN KADAR KAFEIN DALAM KOPI
Teks penuh
Gambar



Dokumen terkait
Penelitian hukum normatif adalah penelitian hukum dengan hanya mengolah dan mengunakan data- data sekunder yang berkaitan dengan “ Tinjauan Hukum Fungsi Yayasan yang Didirikan
The direction-dependent window surface numbers A F,i are replaced by the total window surface A F and the direction-dependent global radiation values are replaced
merencanakan kegiatan tindak lanjut dalam bentuk pembelajaran remedi, program pengayaan, layanan konseling dan/atau memberikan tugas baik tugas individual maupun kelompok
pada hutan produksi yang melakukan pelanggaran terhadap ketentuan sebagaimana dimaksud dalam Pasal 20, Pasal 71 huruf a, huruf b angka 3), huruf f, huruf i, Pasal 73 ayat (5)
Penerbitan jurnal membutuhkan pengelolaan data yang baik dan dapat dengan mudah digunakan oleh pengguna (reviewer dan redaksi), hal ini dapat diwujudkan dengan penggunaan Sistem
o. Pelaksanaan tugas-tugas lain yang diberikan Walikota sesuai dengan bidang tugasnya. Berdasarkan Peraturan Daerah Nomor 04 Tahun 2013 tentang Perubahan
Secara tidak langsung, sikap ( attitude ), norma subjektif ( subjective norm ) dan pengetahuan halal ( halal knowledge ) masyarakat muslim tidak berpengaruh
Rasa syukur kehadirat Allah SWT, yang telah melimpahkan rahmat dan Ridho-Nya kepada saya sehingga dapat menyelesaikan Tugas Akhir dengan judul PENDEKATAN