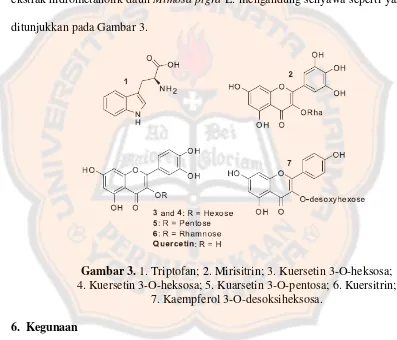
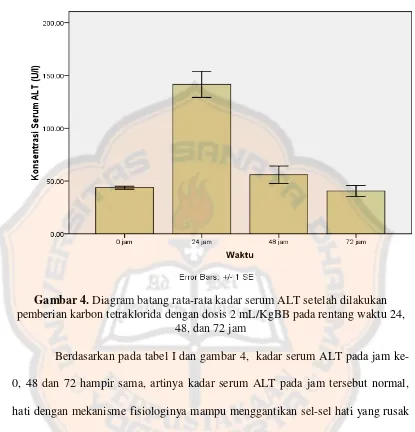
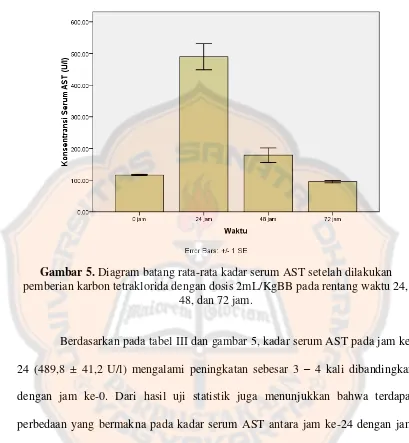
Efek hepatoprotektif pemberian infusa herba mimosa pigra l. selama enam hari pada tikus jantan terinduksi karbon tetraklorida - USD Repository
Teks penuh
Gambar




Dokumen terkait
Baku emas pemeriksaan tersebut adalah spektrofotometer , tetapi penggunaan glukometer lebih sederhana , oleh karena itu, tujuan penelitian ini untuk mengetahui
Tujuan penelitian yaitu untuk mengetahui cara pengiriman dan pemesanan barang dari perusahaan ke supplier saat ini berikut perbaikan-perbaikannya dan untuk
Peraturan Pemerintah Nomor 4 Tahun 2001 tentang Pengendalian Kerusakan dan atau Pencemaran Lingkungan Hidup Yang Berkaitan dengan Kebakaran Lahan dan Hutan (Lembaran Negara
menggunakn bahan/barang yang ditemukan di lingkungan tempat tinggal siswa. Melihat penjelasan di atas dapat disimpulkan bahwa KIT IPA merupakan alat yang berguna
Dengan menggunakan media audio secara tepat dan bervariasi dapat mengatasi sikap pasif siswa, lingkungan, kenyataan, dan memungkinkan siswa untuk belajar sesuai dengan
Pembakaran dan pengembangan gas ini terjadi di dalam ruang bakar yang sempit dan tertutup (tidak bocor) dimana bagian atas dan samping kiri kanan dari ruang bakar adalah
Penelitian ini merupakan sebuah penelitian lapangan yang bertujuan untuk mendeskripsikan dinamika pembebasan tanah dalam proyek pembangunan jalan MERR II-C Gunung Anyar dan
“Sebenarnya cara untuk membentuk dan mengembangkan kepribadian santri baik di dalam atau di luar kelas itu sama saja.. Mau tidak mau ya harus dipaksa terlebih dahulu, yang