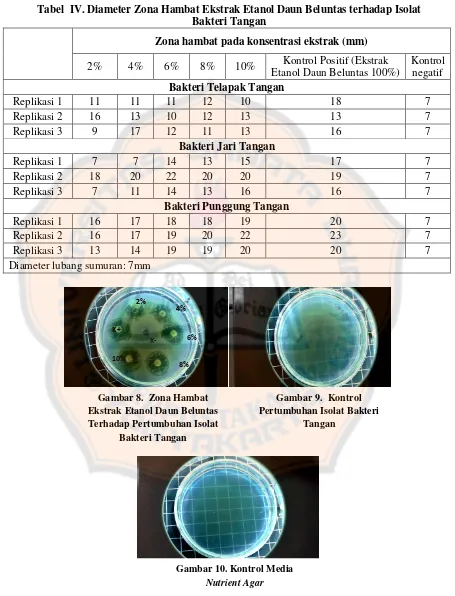
Pengaruh variasi jumlah CMC-Na sebagai gelling agent terhadap sifat fisik dan stabilitas fisik sediaan sabun cuci tangan antibakteri ekstrak etanol daun beluntas (pluchea indica (l.) less) - USD Repository
Teks penuh
Gambar




Dokumen terkait
Kesejajaran tubuh dan postur tubuh yang baik akan menempatkan tubuh pada posisi tubuh yang meningkatkan keseimbangan yang optimal dan fungsi tubuh yang maksimal, baik dalam
Jika dibandingkan dengan standar plastik internasional(ASTM5336) dalam (Averous,2009) besarnya kuat tarik untuk plastik PLA dari Jepang mencapai 2050 MPa dan plastik PCL
sistem pentahanan juga memiliki beberapa syarat agar sistem pentanahan dapat bekerja dengan baik, yaitu, tahanan pentahanan yang digunakan, sistem dapat digunakan untuk
Sumber pendapatan utama rumah tangga petani contoh di Kabupaten Donggala adalah dari usahatani (On-Farm), yang memberi kontribusi sebesar 65,51 persen dari seluruh
Untuk mendapatkan kejelasan hubungan antara penafsiran yang fokus pada ayat-ayat hukum dengan latar belakang penafsir sebagai kritik terhadap tafsir sektarian
Keempat, karena Inggris dan Prancis tahu Liga tidak bisa menghentikan negara-negara agresif, Mereka bukan Diikuti kebijakan peredaan atau memberikan Hitler apa yang ia ingin
1) Pertama, awali dengan motivasi untuk pembinaan hubungan baik. Peneliti/konselor dapat memberikan kegiatan pendahuluan, seperti permainan atau bermain peran, yang
Setelah konselor memberi terapi kepada konseli, langkah selanjutnya evaluasi dan follow up, dalam menindak lanjuti masalah ini konselor melakukan home visit sebagai upaya