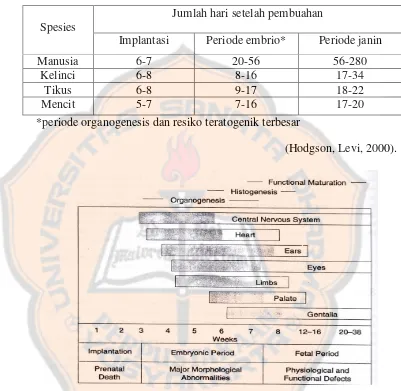
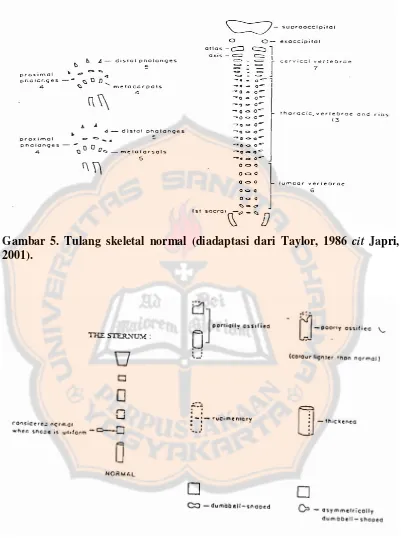
Efek teratogenik ramuan segar jamu kunyit asam pada tikus - USD Repository
Teks penuh
Gambar



Dokumen terkait
Ramai yang menyatakan seksyen A ini adalah satu seksyen yang sengaja diadakan untuk memerangkap calon dan ianya sama-sekali tidak masuk akal kerana skop yang dirangkumi oleh
Dan pada akhirnya pemerintah memutuskan untuk mencabut kembali kebijakan kantong plastik berbayar tersebut, karena menurut Roy N Mandey selaku Ketua umum Aprindo awalnya
Simpulannya adalah ciri-ciri yang paling menonjol bahwa data berstatus sebagai frasa yaitu bersifat renggang/longgar/terbuka, memiliki makna sebenarnya di kedua unsurnya, di
asal, sebagai penggantinya dapat digunakan Surat Pernyataan dari dosen yang bersangkutan yang menyatakan sudah tidak lagi sebagai dosen tetap di P.T.. asal Æ Kopertis akan
Sarung tangan yang kuat, tahan bahan kimia yang sesuai dengan standar yang disahkan, harus dipakai setiap saat bila menangani produk kimia, jika penilaian risiko menunjukkan,
Dengan demikian, untuk hipotesis nul (H 0 ) yang menyatakan tidak terdapat perbedaan kemampuan pemecahan masalah IPA antara kelompok peserta didik yang belajar dengan
Berdasarkan latar belakang permasalahan yang dialami pihak RSISA tersebut, maka setidaknya dibutuhkan sebuah sistem aplikasi yang membantu pengunjung serta karyawan
Secara umum manfaat media pembelajaran adalah memperlancar interaksi antara guru dengan siswa sehingga kegiatan pembelajaran lebih afektif dan efisien.