RESPON SITOKIN PADA KULTUR SEL LIMFOSIT RESPON SITOKIN PADA KULTUR SEL LIMFOSIT SEBAGAI UJI PENTING DALAM PENGEMBANGAN VAKSIN MALARIA IRADIASI - e-Repository BATAN
Teks penuh
Gambar
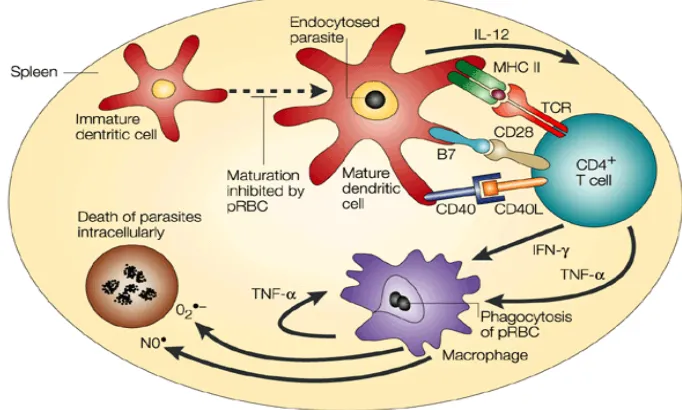
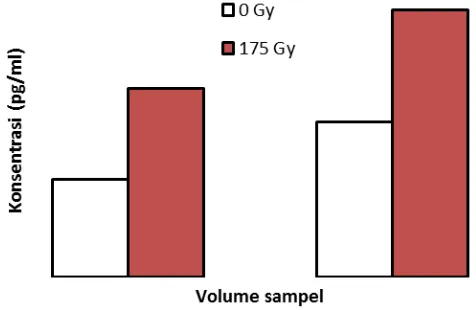
Dokumen terkait
Penelitian hukum ini bertujuan untuk mengetahui bagaimana bentuk perlindungan HAM bagi pekerja disabilitas yang dilakukan pada PT Pertamina Refinery Unit V Balikpapan dan apa saja
Dari pemaparan di atas dapat disimpulkan bahwa fungsi humas dilembaga pendidikan adalah menumbuh dan mengembangkan hubungan yangharmonis melalui komunikasi dengan
Sehubungan dengan hasil refleksi di atas, maka dalam pelaksanaan tindakan pada siklus kedua di- lakukan perbaikan-perbaikan dengan (a) membentuk kelompok didasarkan pada
Syarat membran untuk sel bahan bakar agar dapat bekerja dengan baik adalah memiliki konduktivitas yang besar dan tahan terhadap suhu operasi tinggi.. Suhu operasi tinggi
Material hasil sintesis dikarakterisasi dengan menggunakan XRD, FTIR, SEM, TGA dan dilakukan uji aktivitas katalis pada reaksi esterifikasi PFAD untuk menurunkan kadar Free
Intan Pariwara semakin membuktikan signifikansi teori dan juga para peneliti terdahulu yang digunakan sebagai referensi dalam penelitian ini, khususnya dari segi
[r]
Jilid kawat ini umumnya dipergunakan untuk menjilid buku, majalah, tabloid, brosur yang jumlah halamanya tidak lebih dari 100 halaman. Bisa dikerjakan dengan jalan manual