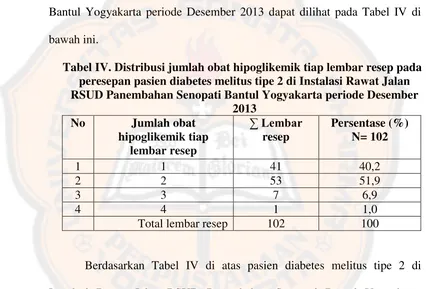
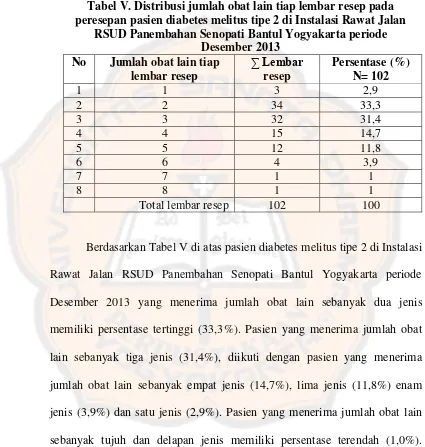
Studi literatur interaksi obat pada peresepan pasien diabetes melitus tipe 2 di Instalasi Rawat Jalan RSUD Panembahan Senopati Bantul Yogyakarta periode Desember 2013 - USD Repository
Teks penuh
Gambar


Dokumen terkait
[r]
Peraturan Menteri Negara Koperasi Nomor 19 tahun 2008 tentang Pedoman Pelaksanaan Kegiatan Usaha Simpan Pinjam oleh
[r]
463 Penyusun Program Peningkatan Kualifikasi Pendidikan Dalam Negeri Kementerian Riset, Teknologi, dan Pendidikan Tinggi 7 4 464 Penyusun Program Peningkatan Kualifikasi Pendidikan
Dalam kegiatan pemeliharaan suatu perusahaan merupakan persoalan yang menyangkut usaha-usaha untuk menghilangkan kemungkinan–kemungkinan yang menimbulkan kemacetan yang
Perhitungan pada metode tenaga kerja berubah di atas kemudian akan digunakan untuk perhitungan ongkos produksi metode tenaga kerja berubah, dimana pada
Tujuan dari penelitian ini adalah untuk mengetahui perubahan luas lahan mangrove yang terjadi di kawasan pesisir Desa Bedono, Kecamatan Sayung, Kabupaten Demak
mengeksploitasi Migas Natuna, tetapi juga harus segera membangun armada kapal penangkap ikan yang tangguh dan professional di Natuna, Armada ini harus bermarkas di Natuna,