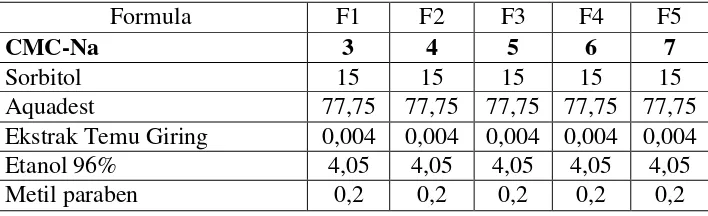
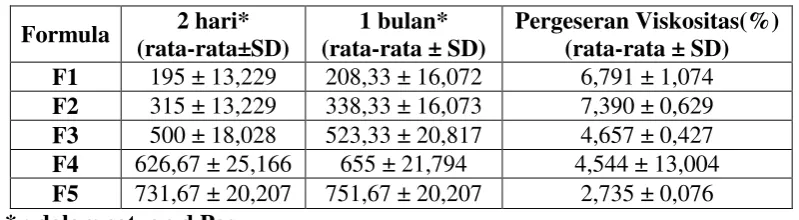
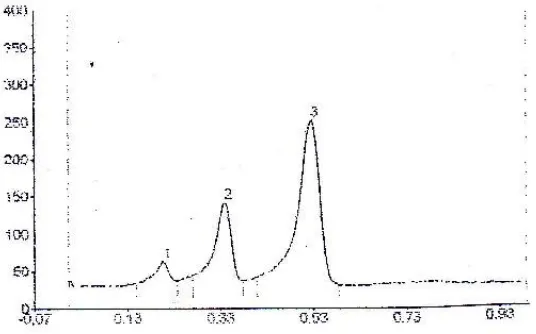
Pengaruh penambahan konsentrasi CMC-Na pada sediaan sunscreen gel ekstrak temu giring (Curcuma heyneana Val.) terhadap sifat fisik dan stabilitas sediaan dengan sorbitol sebagai humectant - USD Repository
Teks penuh
Gambar
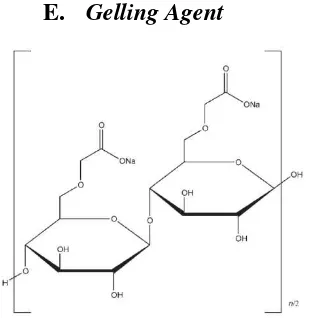
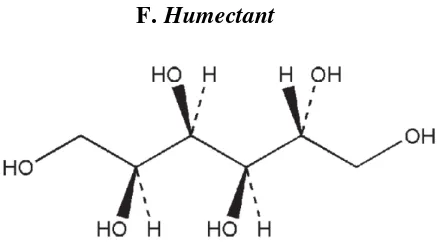

Dokumen terkait
Berdasarkan hasil yang diperoleh pada penelitian ini, dapat disimpulkan bahwa terdapat perbedaan kadar fenolik total sari rimpang temu giring ( Curcuma heyneana )
Skripsi yang berjudul “Pengaruh berbagai konsentrasi hydroxy propyl methyl cellulose sebagai bahan salut selaput terhadap mutu tablet rimpang temu giring (
Pada penelitian ini dilakukan uji daya antibakteri terhadap fraksi kloroform rimpang temu giring (Curcuma heyneana Val. Zijp.) dengan metode difusi agar menggunakan
Efek Immunodulator Ekstrak Rimpang Temu Giring (Curcuma heyneana Valeton & Zijp.) Terhadap Respon Hipersensitivitas Tipe Lambat DAN Titer Antibodi Sel Imun
UJI EFEK ANTIINFLAMASI EKSTRAK ETANOL RIMPANG TEMU GIRING ( Curcuma heyneana Val & Zijp) TERHADAP TIKUS YANG. DIINDUKSI
Pengaruh Ekstrak Rimpang Temu Giring (Curcuma heyneana Valeton & zijp.) Terhadap Aktivitas Fagositosis pada mencit Jantan.. Medan: Fakultas Farmasi Universitas
Berdasarkan hasil penelitian yang telah dilakukan karakteristik sediaan serum wajah dengan variasi konsentrasi sari rimpang temu giring ( Curucuma heyneana ) terfermentasi
Dekokta rimpang temu giring (curcuma heyneana Val & Zijp) mempunyai efek tonikum pada mencit jantan galur swiss webster. Perlu dilakukan penelitian lebih lanjut terhadap