Myasthenia Gravis
Teks penuh
Gambar

Garis besar
Dokumen terkait
2 Myasthenia gravis dapat menyebabkan kelemahan pada kelopak mata dan otot-otot mata pada hingga 90% kasus; setengah dari pasien tersebut menunjukkan gejala
4 Romi dkk mengatakan bahwa Miastenia gravis (MG) adalah penyakit autoimun yang ditandai dengan kelemahan patologis yang berfluktuasi dengan remisi dan
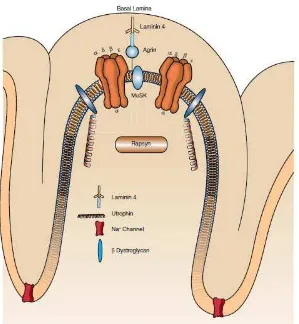
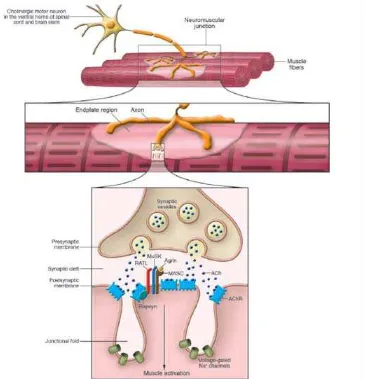
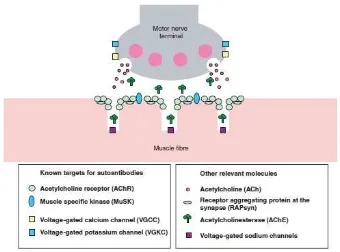
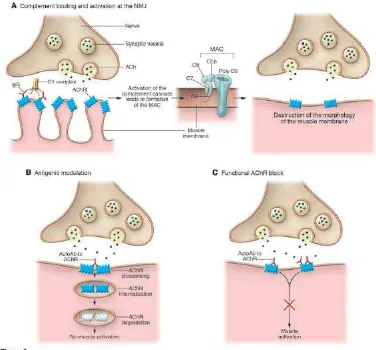
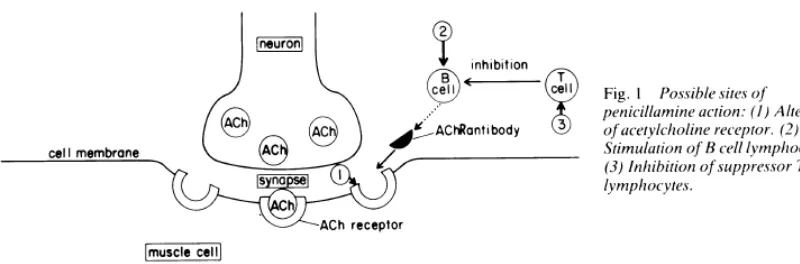
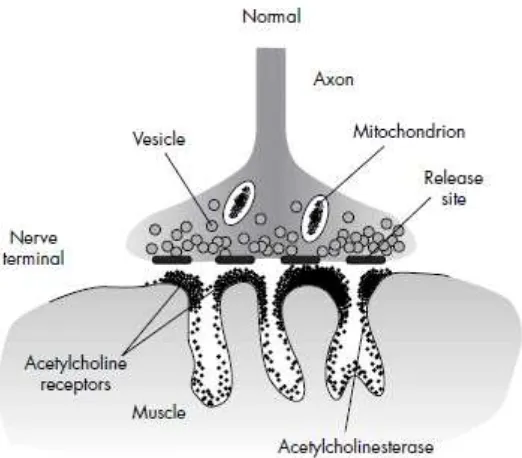
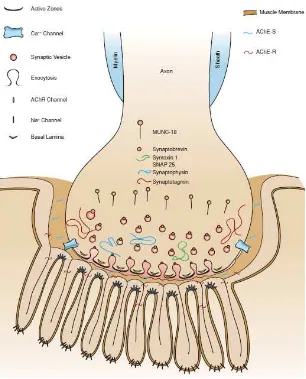
Miastenia gravis adalah penyakit autoimun yang menyerang neuromuskular juction ditandai oleh suatu kelemahan otot dan cepat lelah akibat adanya antibodi
Seperti pada penyakit autoimun lainnya, tidak ada yang dapat dilakukan untuk mencegah terjadinya myasthenia gravis, karena bukan disebabkan oleh sesuatu yang bisa kita
Myasthenia gravis merupakan penyakit dengan kelemahan otot yang parah dan satu-satunya penyakit neuromuscular dengan gabungan antara cepatnya terjadi kelelahan otot-otot
Myasthenia gravis merupakan penyakit dengan kelemahan otot yang parah dan satu-satunya penyakit neuromuscular dengan gabungan antara cepatnya terjadi kelelahan otot-otot
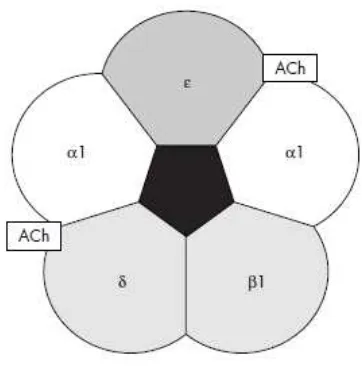
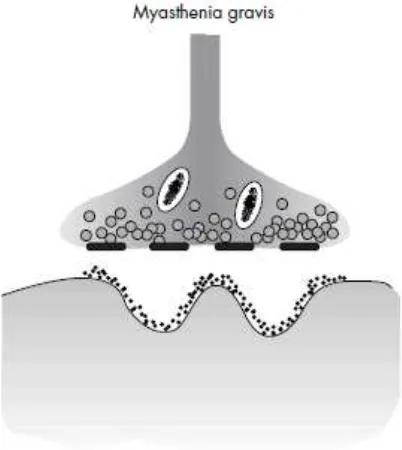
Pada myasthenia gravis, sistem kekebalan menghasilkan antibodi yang menyerang salah satu jenis reseptor pada otot samping pada simpul neuromukular- reseptor yang
Apabila sudah meningkat pada klasifikasi yang lebih berat, maka gejala yang muncul dapat berupa kelemahan pada leher, ekstrimitas, hingga otot- otot pernapasan seperti sesak atau bahkan