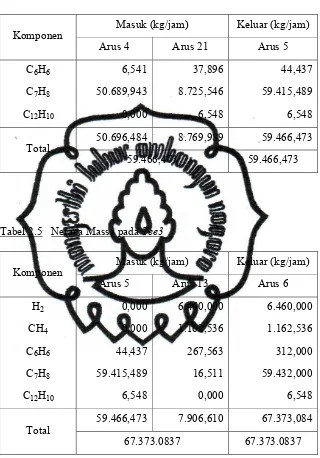
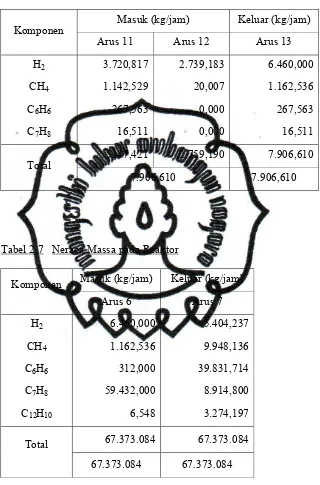
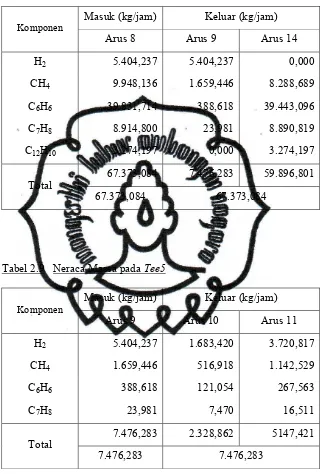
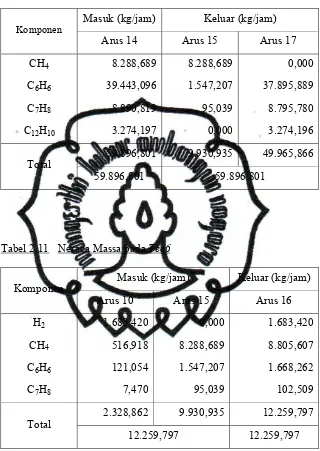
PRARANCANGAN PABRIK BENZENE DARI TOLUENE DAN HIDROGEN KAPASITAS 300.000 TON TAHUN
Teks penuh
Gambar
Dokumen terkait
Industri PTA merupakan pengkonsumsi asam asetat terbeasr yang digunakan sebagai media pelarut katalis. Industri etil asetat sebagai bahan
Prarancangan Pabrik Monochlorobenzene dari Benzene dan Chlorine Kapasitas 175.000 ton/tahun..
Sodium Styrene Sulfonate merupakan bahan kimia yang digunakan sebagai resin penukar ion, bahan penolong dalam produksi Polyester Fiber serta bahan penolong
Ethyl Chloride merupakan bahan kimia yang digunakan dalam bidang industri obat-obatan, refrigerant , dan bahan pembuat senyawa organik digunaka n sebagai bahan
Asam akrilat digunakan sebagai bahan baku untuk pembuatan senyawa. ester
sebagai bahan baku pembuatan bisfenol-A yang digunakan dalam industri plastik, bahan baku industri kaprolaktan yang digunakan dalam pembuatan nilon dan bahan baku dalam
Proses produksi high impact polystyrene menggunakan proses bulk polymerization continue dengan bahan baku yaitu styrene sebagai monomer, polybutadiene sebagai rubber,
1-bromopropana digunakan secara luas dalam berbagai bidang antara lain: sebagai pelarut organik yang bermanfaat sebagai bahan pembersih permukaan logam, membersihkan