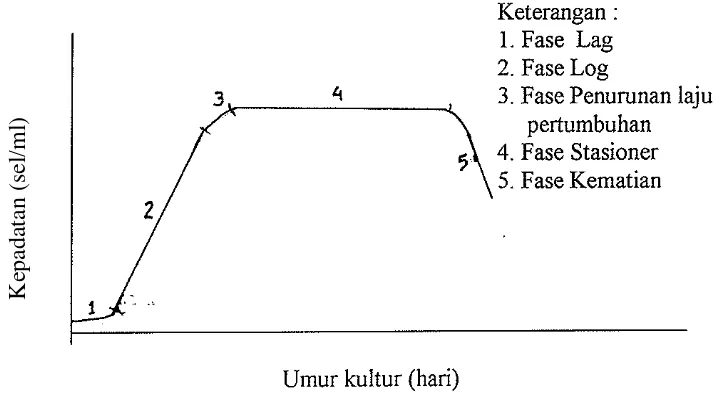
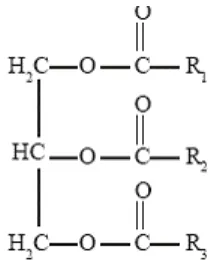
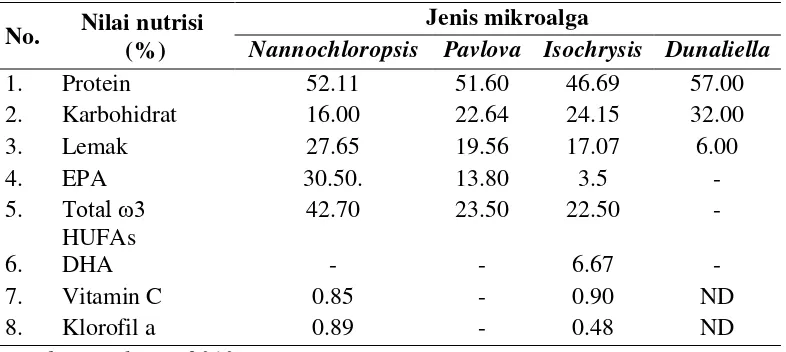
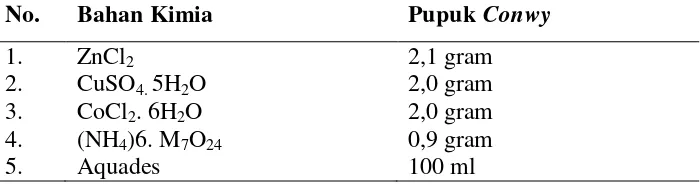
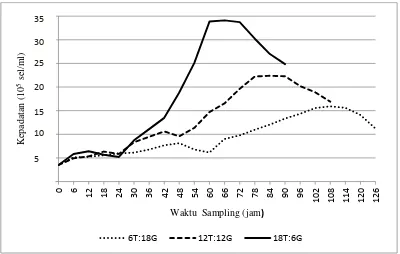
Kandungan Lemak Total (Crude Lipid) Nannochloropsis sp. Pada Fotoperiod Yang Berbeda
Teks penuh
Gambar


Dokumen terkait
Hanya saja, ada satu riwayat dari Ibn Jarir dan Ibn Mundzir, atas Ibn Jarir, yang menjelaskan bahwa dalam peristiwa ayat ini tidak sebatas dari Ahl al-Kitâb ; Yahudi saja,
Hubungan tersebut menunjukkan bahwa pertambahan panjang total lebih cepat dari pada pertambahan karakter morfometrik pembandingnya, sedangkan pada ikan buntal mas
NO HARI/ TGL JAM PUKUL JURUSAN SMT-KLS MATAKULIAH DOSEN PEMBINA PENGAWAS RUANG Bahasa dan. sastra Arab VI A & B Nadzariyah al-Adab II Dr.H.Helmi Syaifuddin,M.Fil.I
“(keperawatan adalah) : seni humanistic yang dapat dipelajari dan ilmu yang berfokus pada personalisasi perilaku asuhan (individu dan kelompok), fungsi, dan proses yang diarahkan
Sedangkan data kuantitatif berupa perhitungan indikator penyimpanan yang meliputi Turn Over Ratio (TOR), persentase obat hampir kadaluarsa dan persentase obat
Tujuan dalam penelitian ini adalah untuk mengetahui apakah ada pengaruh yang signifikan antara kompetisi dalam kegiatan belajar ekonomi terhadap motivasi belajar
Bahwa Lembaga PAUD/Organisasi/Yayasan Pendidikan yang namanya tercantum dalam lampiran surat keputusan ini telah memenuhi syarat untuk menerima bantuan Dana
Kepadatan Anopheles tertinggi (4,1 ekor/orang/ jam) pada kelembaban udara 85,3 % dan terrendah 1,0 ekor/orang/jam pada saat kelembaban udara 78,5% dan 76,0% dengan