Pre-Treatment of Raw Water Using Fixed Bed Reactor Technology
Teks penuh
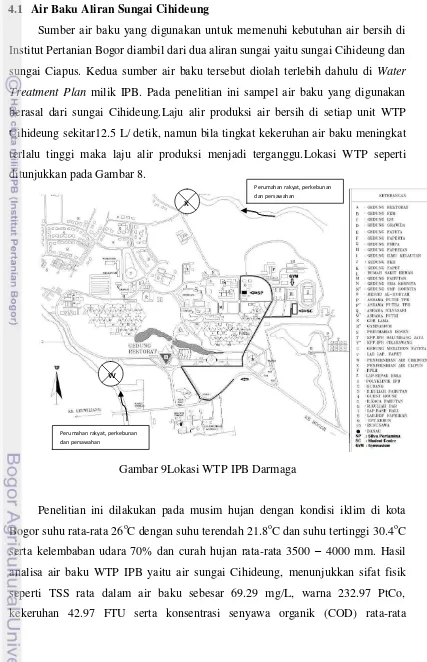
Gambar
Garis besar
Dokumen terkait
Pola reaksi perubahan nitrit isolat NOB H1 (Gambar 3) menunjukkan bahwa secara umum terjadi penurunan konsentrasi nitrit yang diikuti oleh kenaikan konsentrasi amonium dan
Tugas akhir dengan judul “Pengembangan Aplikasi Pembelajaran Lapisan Tanah untuk Anak SD Berbasis Multimedia (Platasia)” yang ditulis untuk memenuhi.. persyaratan
Ideologi kebangsaan yang tumbuh dan berkembang melalui proses sejarah dalam kesadaran antarkaum terpelajar Indonesia pada akhirnya dapat menjadi bagian integral
Bercermin dari sosok JK, penulis menekankan bahwa kewirausahaan yang mampu memberdayakan umat merupakan bagian dari jihad. Point inti dari jihad di era damai saat ini
Hal ini dibuktikan dengan hasil statistik uji t variabel Perceived of Risk diperoleh nilai signifikansi sebesar 0,000, dan koefisien regresi mempunyai nilai negatif
Penelitian menggunakan rancangan acak lengkap non faktorial dengan 13 perlakuan yang diulang sebanyak 3 kali, yaitu kontrol (tanpa inokulasi), inokulasi 300 Rs,