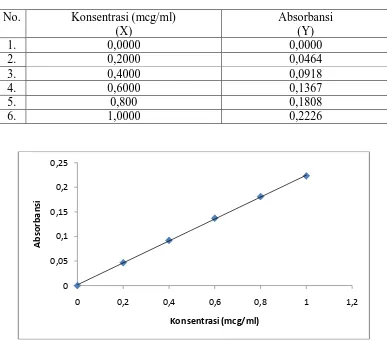
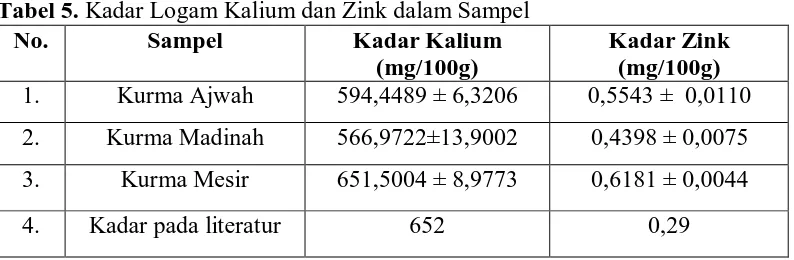
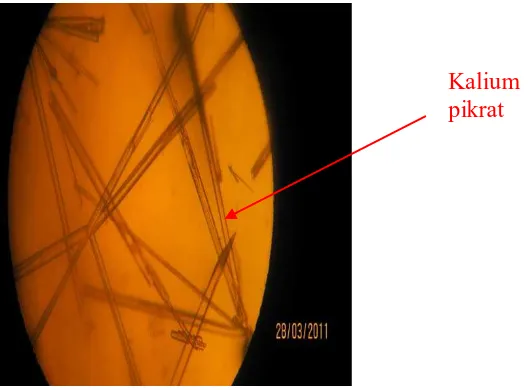
Penetapan Kadar Kalium (K) Dan Zink (Zn) Pada Buah Kurma (Phoenix dactylifera L.) Secara Spektrofotometri Serapan Atom
Teks penuh
Gambar
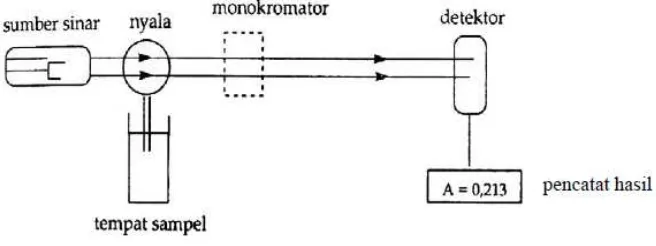
Dokumen terkait
2 Hadis di atas adalah merupakan dalil yang digunakan oleh para sufi untuk menjastifikasi tafsir mereka yang eksentrik, menurut mereka dibalik makna zahir dalam redaksi
Ibu Dwi Sulistyowati, S.Pd dan Ibu Titik Susilowati, S.Pd selaku guru mata pelajaran Fisika SMP Negeri 1 Jaten yang telah memberikan waktu untuk membantu penulis
Berdasarkan pada latar belakang yang telah diuraikan di atas, maka rumusan masalah penelitian ini adalah “Adakah beda motivasi kerja perawat antara gaya Kepemimpinan Demokratik
We aim at providing images of vegetation indices in rather high spatial resolution (comparing to satellite sensors) for optical remote sensing. Our acquisition system has to be
Berdasarkan hasil penelitian yang telah dilakukan tentang “Pengaruh Penyuluhan Kanker Serviks terhadap Pengetahuan dan Sikap Ibu Melakukan Deteksi Dini Inspeksi
Rata-rata n-gain keterampilan me- nentukan langkah kerja pada materi larutan elektrolit dan non-elektrolit pada kelas yang diterapkan LKS berbasis inkuiri terbimbing
Salah satu Produk De Nature adalah Ambejoss yang terbuat dari ekstrak daun ungu, mahkota dewa, kunyit putih Sedangkan Salep salwa dibuat dengan campuran propolis murni,
Intervensi yang di berikan pada klien sesuai dengan NIC 2015 mengenai gangguan pertukaran gas adalah dengan memonitor status nafas klien, dan mengajarkan nafas dalam dan teknik