reaksi titrasi Kelas11 kimia2
Teks penuh
Gambar

Garis besar
Dokumen terkait
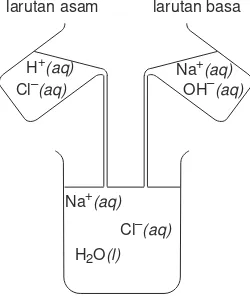
konsentrasi HCl tersebut melalui suatu prosedur yang disebut titrasi, dimana kita menetralisasi suatu asam dengan suatu basa yang telah diketahui konsentrasinya.. Pada
4.2 Menghitung banyaknya pereaksi dan hasil reaksi dalam larutan elektrolit dari hasil titrasi asam dan basa. C4 ¾ Menuliskan reaksi dalam bentuk ion
Penyelesaian:.. 18,115 mL basa digunakan untuk mentitrasi 25,0 mL asam sampai titik akhir titrasi. a) Hitunglah konsentrasi larutan basa. b)Hitunglah massa molar larutan
Untuk membantu mengamati titik akhir titrasi asam basa, dapat digunakan indikator tertentu yang berupa asam atau basa lemah yang memiliki zat warna yang berbeda dalam
Senyawa asam dapat ditentukan konsentrasinya dengan cara menitrasi larutan tersebut dengan larutan standart basa, dengan menggunakan indikato PP untuk menentukan titik
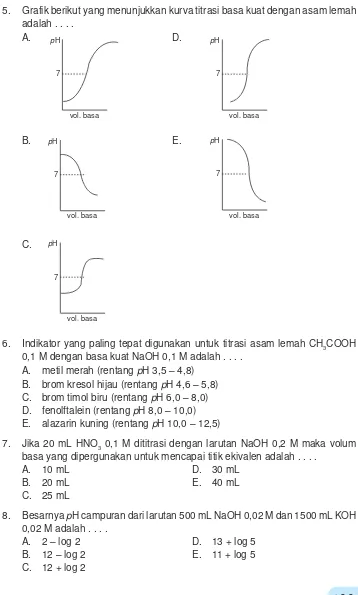
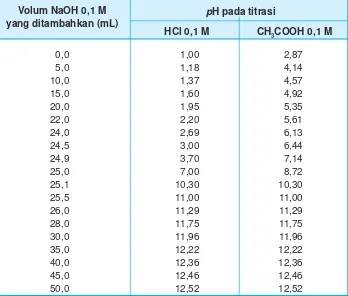
Titik akhir titrasi diharapkan mendekati titik ekuivalen titrasi, yaitu kondisi pada saat larutan asam habis bereaksi dengan larutan basa.. Pendekatan antara titik akhir titrasi
Larutan baku yang digunakan pada titrasi netralisasi adalah asam kuat atau basa kuat, karena zat-zat tersebut bereaksi lebih sempurna dengan analit dibandingkan dengan jika
Siswa dibimbing untuk menentukan konsentrasi larutan asam atau basa berdasarkan data hasil titrasi asam basa. 5) Fase V: Evaluation.. Siswa mengerjakan kuis yang