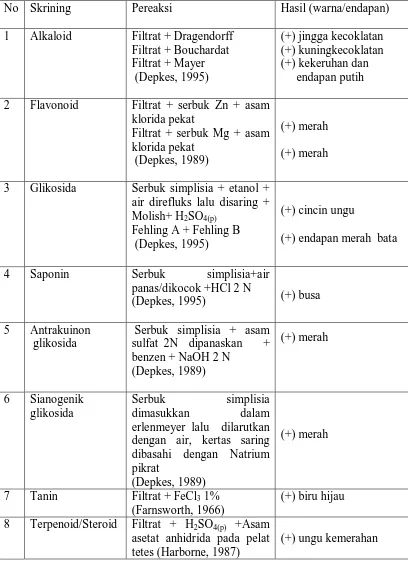
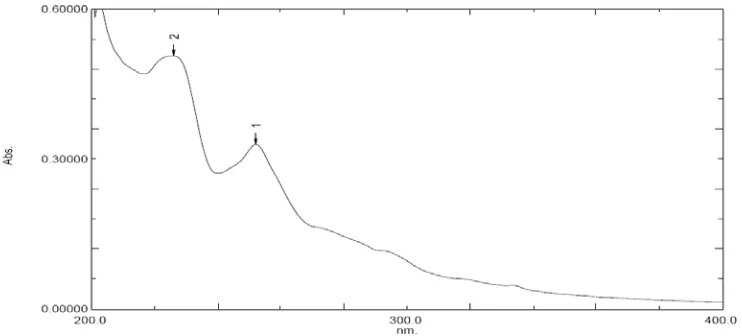
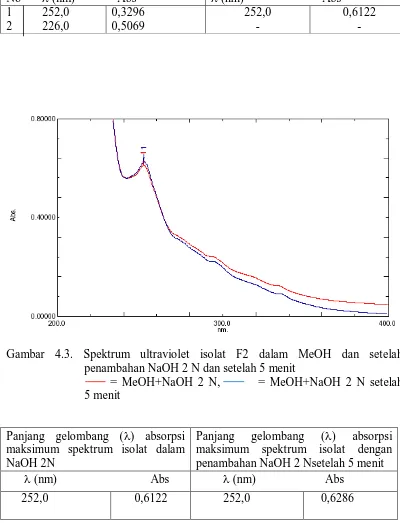
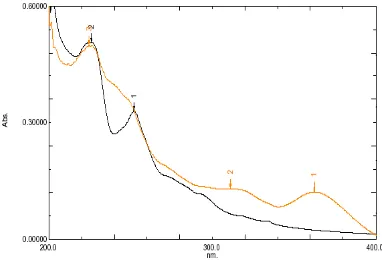
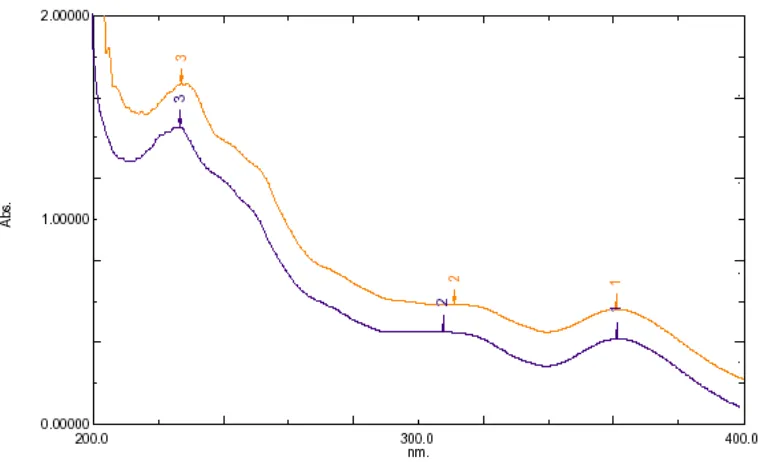
Isolasi dan Karakterisasi Senyawa Flavonoid Umbi dari Tumbuhan Bawang Sabrang (Eleutherine palmifolia (L) Merr)
Teks penuh
Gambar

Dokumen terkait
Saat pasien dirawat dirumah sakit lain ataupun memeriksakan kesehatan di dokter praktek lain, dokter bisa memberikan penanganan yang tepat, sesuai dengan riwayat
Dalam memastikan ujian yang dijalankan sesuai untuk mengukur tahap ketinggian rejaman bagi pemain yang berposisi perejam dalam sepak takraw, pengkaji telah membuat satu ujian
Indikator-indikator motivasi kerja dan gaya kepemimpinan apa saja yang berpengaruh terhadap produktivitas kerja pegawai pada Deputi Bidang Pengkajian dan Penanganan Sengketa dan
Dari lima formula yang dibuat, formula dengan perbandingan tween 80 dan gliserin = 3,75 mL : 1,25 mL ditemukan sebagai formula terbaik.Mouthwash daun kemangi menunjukkan
Pemberian ekstrak etanolik jeruk nipis ( Citrus aurantifolia ) terbukti dapat menekan karsinogenesis melalui penekanan ekspresi c-Myc dan penghambatan proliferasi pada
Bebas Premi untuk Bayi Baru Lahir: Bayi baru lahir berhak untuk mendapatkan perlindungan asuransi yang sama dengan Tertanggung setelah 15 hari dari tanggal kelahiran atau tanggal
Berdasarkan uraian kondisi yang terjadi di Bank BRI, maka permasalahan yang diangkat dalam penelitian ini yaitu bagaimana cara meningkatkan pengambilan keputusan menabung
Terumbu karang di perairan laut Desa Stardas telah mengelami kerusakan dengan tutupan karang hidup relatif rendah yaitu 27.73 %. Ada kecenderungan persentasi tutupan