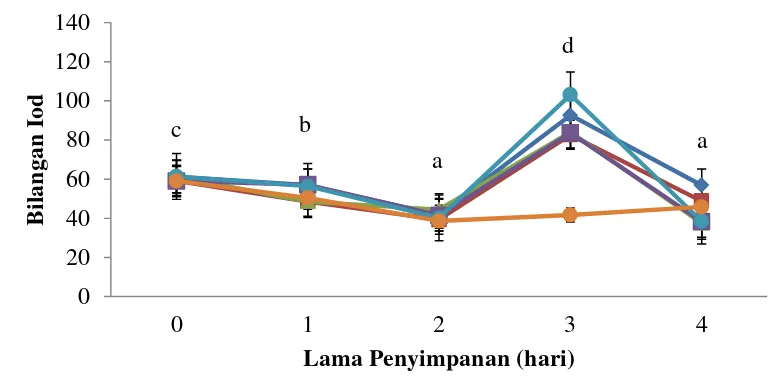
Stabilitas Kapsul Minyak Ikan Patin (Pangasius sp.) selama Penyimpanan dengan Metode Schaal
Teks penuh
Gambar

Dokumen terkait
Daktilitas adalah kemampuan suatu struktur gedung untuk mengalami simpangan pasca elastik yang besar secara berulang kali dan bolak balik akibat beban gempa di atas beban gempa
Hipotesis merupakan dugaan sementara yang diajukan peneliti mengenai permasalahan yang muncul dalam lingkungan dan berdasarkan rumusan masalah hipotesis
a) Dengan naiknya derajat korelasi di antara variabel-variabel bebas, penaksir-penaksir OLS masih bisa diperoleh, namun kesalahan- kesalahan baku (standard
Upah tenaga kerja langsung (bagian produksi) dan biaya :
1) Hasil tes HIV negatif sebelumnya. 2) Atau hasil tes HIV negatif pada saat diagnosa tuberculosis. Catatan : apabila pada pemeriksaan selanjutnya ternyata hasil tes HIV menjadi
Gopher Perangkat yang memungkinkan pemakai untuk menemukan informasi yang terdapat pada server gopher melalui menu yangh bersifat hierarkis Archie Perangkat yang dapat digunakan
menyelesaikan model matematika yang telah dibuatnya; c) Kesalahan melaksanakan rencana, dilihat dari hasil pekerjaan siswa yaitu ketika siswa tidak menyelesaikan model
Dimana ketika sosialisasi pajak yang diberikan oleh DJP dapat terselenggara secara efektif dan tepat sasaran sebagai bentuk penambahan pengetahuan pajak, kemudian