Karakterisasi Simplisia dan Uji Aktivitas Antioksidan Ekstrak n-Heksan, Etil Asetat dan Etanol Daun Muda Dari Labu Siam (Sechium edule (Jacq.) Sw.) Dengan Metode DPPH
Teks penuh
Gambar

Dokumen terkait
Senyawa fenolik yang terkandung dalam tanaman, khususnya asam fenolat dan flavonoid, telah diketahui memiliki aktivitas antioksidan yang dapat menghambat radikal bebas dan
Dari hasil penelitian dapat diambil kesimpulan, kondisi optimum ekstraksi senyawa total fenolik buah labu siam menggunakan RSM diperoleh pada waktu ekstraksi 2 jam, nisbah
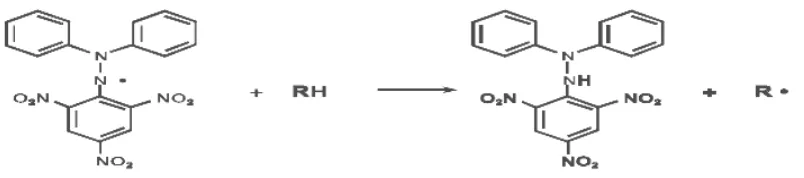
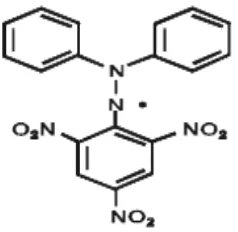
DPPH yang berperan sebagai radikal bebas akan bereaksi dengan senyawa antioksidan, sehingga DPPH akan berubah menjadi diphenilpycrilhydrazine yang bersifat non-
Histopatologi Pankreas Tikus pada Kondisi Diabetes Melitus Resisten Insulin (Hari ke-9) dengan Perbesaran 100x (I) dan 400x (II), pewarnaan H&E. Pulau Langerhans)
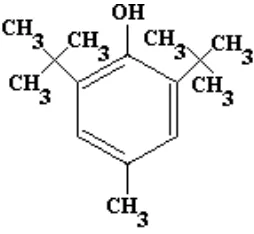
Salah satu metode yang digunakan dalam pengujian zat antioksidan adalah metode DPPH 1,1 difenil-2-pikrilhidrazil yang merupakan radikal bebas, jika direaksikan dengan ekstrak
Antioksidan merupakan suatu senyawa yang berfungsi untuk melindungi sel dari efek berbahaya radikal bebas oksigen yang berasal dari metabolismetubuh maupun faktor
Histopatologi Pankreas Tikus pada Kondisi Diabetes Melitus Resisten Insulin (Hari ke-9) dengan Perbesaran 100x (I) dan 400x (II), pewarnaan H&E. Pulau Langerhans)
Pemberian antioksidan pada pengobatan diabetes tidak hanya diperlukan untuk mencegah kerusakan oksidatif dengan memperbaiki sel β-pankreas yang rusak akibat radikal bebas,