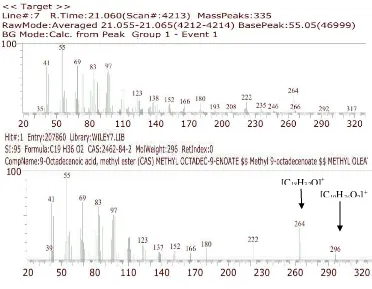
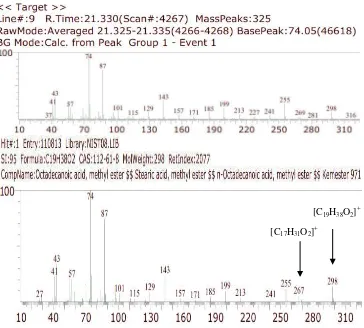
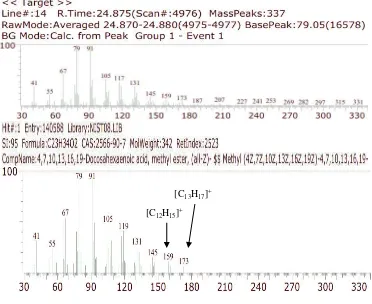
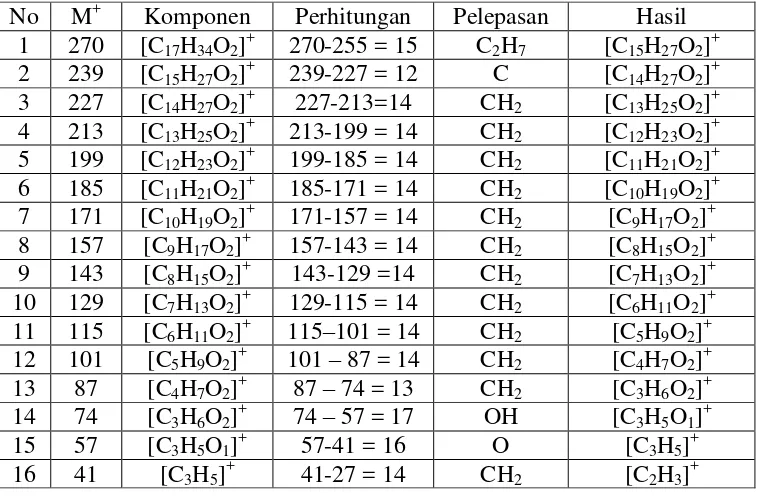
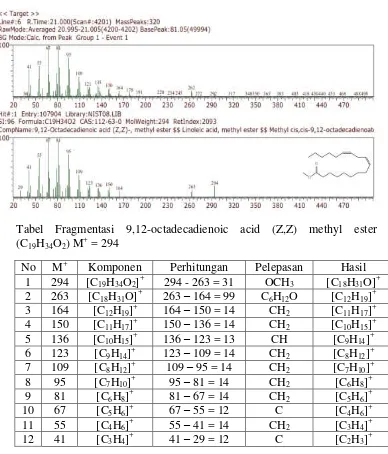
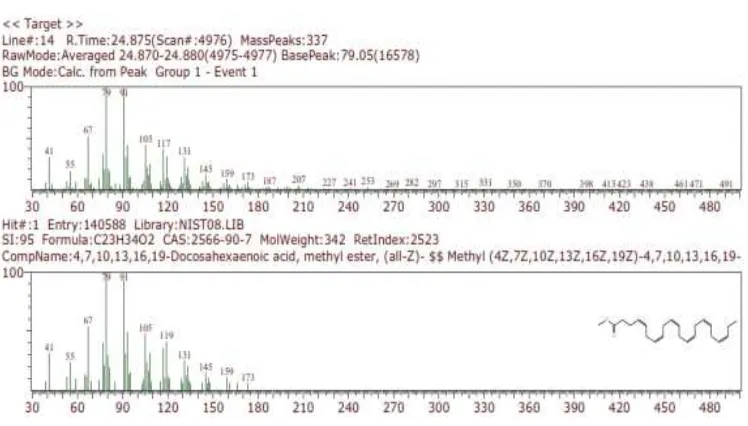
Analisa Komponen Asam Lemak pada Minyak Ikan Nila (Oreochromis niloticus) Secara GCMS
Teks penuh
Gambar
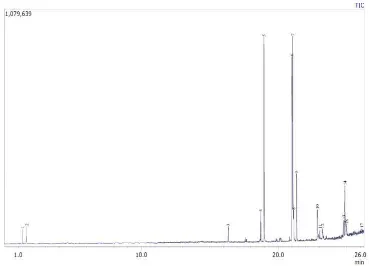
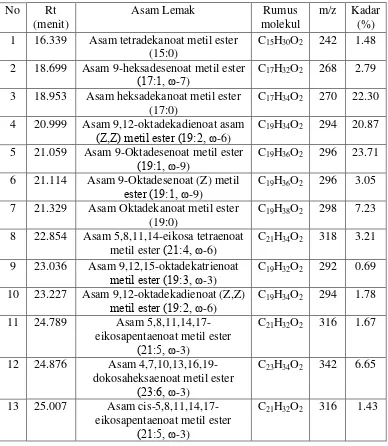
Dokumen terkait
Itlenyediakan informasi dan instruksi yang telah diserahkan otoritas padanya kepada kapal-kapal (dan allied servrbes) sesuai dengan jenis layanan yang ditentukan pada
eksak dengan melihat jumlah paket yang telah diterima selama rentang waktu dilakukannya simulasiDengan demikian dapat dikatakan, untuk membandingkan varian TCP
Kalbant apie kalbinių įgūdžių vystymąsi besimokant bendradarbiavimo būdu, 89% respondentų nurodė, kad vystosi kalbėjimo įgūdžiai, 74% apklaustųjų dar nurodė ir
Kelompok tersebut dapat membantu remaja untuk mengetahui dirinya dalam perbandingan dengan orang lain sehingga mereka dapat membandingkan dirinya dengan kelompoknya,
Atom karbon misalnya memiliki 6 elektron dan juga 6 proton.Selain proton inti atom juga mengandung bagian yang secara listrik bersifat netral, yang biasa disebut
78 percakapan hanya sebatas interaksi secara lisan antara orang yang berbicara (penutur) dengan orang yang diajak berbicara (petutur) yang membahas suatu hal dalam satu
Pengendalian secara teknis dapat dilakukan pada sumber bising, media yang dilalui bising dan jarak sumber bising terhadap pekerja. Pengendalian bising pada sumbernya