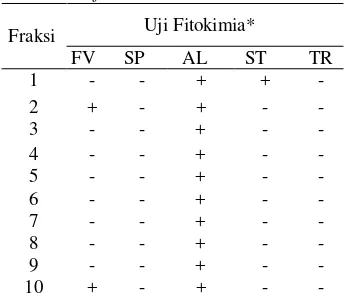
Aktivitas antibakteri fraksi aktif daun lidah mertua (Sansevieria trifasciata Prain)
Teks penuh
Gambar


Dokumen terkait
The findings were compared with those from biogas (containing inhibitors) at lower (reduced) pressures, with inhibitorless gases at atmospheric pressure (1atm), and with
Wasir >> Penyakit ini dapat disebut juga dengan hemoroid atau ambeien, yakni pembesaran pembuluh darah vena yang menjadi rapuh pada daerah rektum (sisi dalam
Perusahaan telah memilih untuk menggunakan model biaya sebagai kebijakan akuntansi pengukuran aset tetapnya; oleh karenanya, saldo selisih penilaian kembali aset
UndangUndang Nomor 32 Tahun 2004 tentang Pe merintahan Daerah (Lembaran Negara Republik In
7.1 Mempraktikkan variasi dan kombinasi teknik dasar salah satu permainan dan olahraga beregu bola besar lanjutan dengan koordinasi yang baik serta nilai kerjasama,
Kombinasi teknik dasar memegang stick dan pukulan (swing/bunch ) 16. Bermain dengan Tennis AZ-ZAHRA-KKM.. Variasi dan kombinasi teknik dasar memegang raket untuk
Menimbang : a. bahwa dalam rangka memenuhi dan mencukupi biaya operasional dan perawatan kapal penyeberangan lintas Sadai-Tanjung Ru dan guna meningkatkan
dimaksud dengan Penanaman Modal Asing adalah kegiatan menanam modal untuk melakukan usaha di wilayah Republik Indonesia yang dilakukan oleh penanam