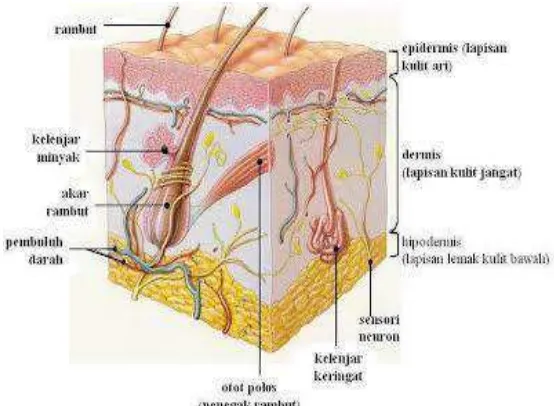
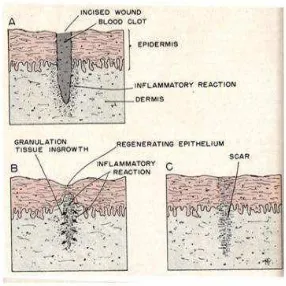
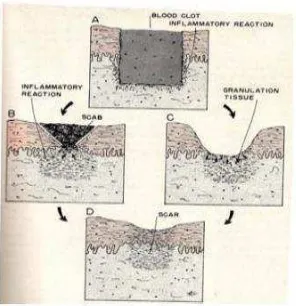
Uji Efektivitas Gel Ekstrak Etanol daun Gulma Siam (Chromolaena odorata) terhadap Penyembuhan Luka Sayat
Teks penuh
Gambar

Dokumen terkait
Penyusunan Rencana Strategis (RENSTRA) Kantor Penanaman Modal dan Pelayanan Perizinan Terpadu Kabupaten Pesisir Selatan Tahun 2011- 2015 yang merupakan tugas sektoral dari
Pembangunan telah menetapkan Undang-Undang Nomor 25 Tahun 2004 tentang Sistem Perencanaan Pembangunan Nasional dan Undang-Undang Nomor 17 Tahun 2007 tentang Rencana Pembangunan
Pertanyaan utama yang akan dijawab melalui penelitian ini adalah apakah penerapan metode bernyanyi dapat meningkatkan prestasi belajar anak didik dalam meningkatkan
Menurut UU no 26 Tahun 2000 tentang pengadilan HAM, Pelanggaran HAM adalah setiap perbuatan seseorang atau kelompok orng termasuk aparat negara baik disengaja atau
[r]
Pada hari ini Jumat tanggal dua puluh delapan bulan Desember tahun dua ribu dua belas, melalui website LPSE Kementerian Keuangan www.lpse.depkeu.go.id telah dilaksanakan
If any offer of securities is made, it shall be pursuant to a definitive final offering circular (the “Offering Circular”) prepared by or on behalf of the DBS Group which would
Bagi usaha kecil dan menengah (UKM), keberhasilan dalam pengembangan inovasi produk menunjukkan bahwsa UKM sudah selangkah lebih maju dibanding dengan