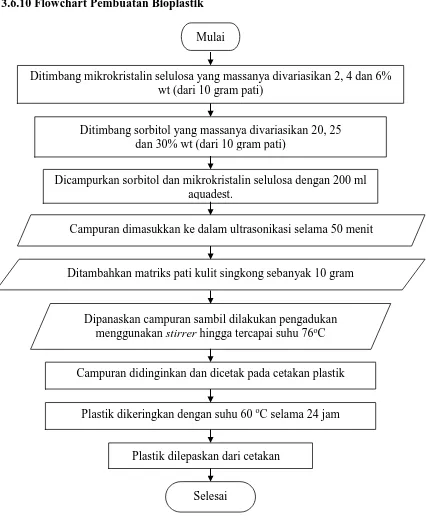
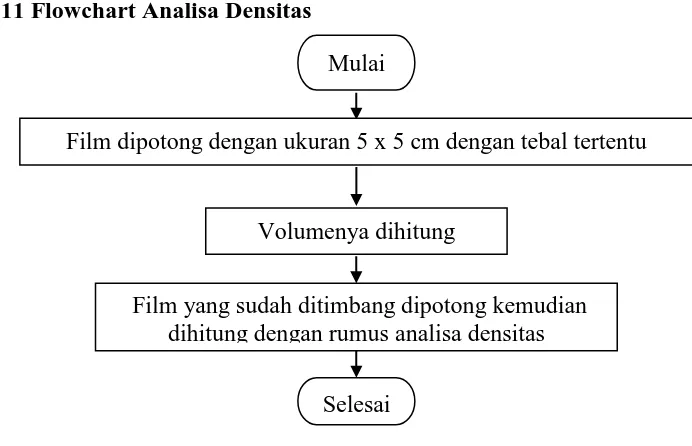
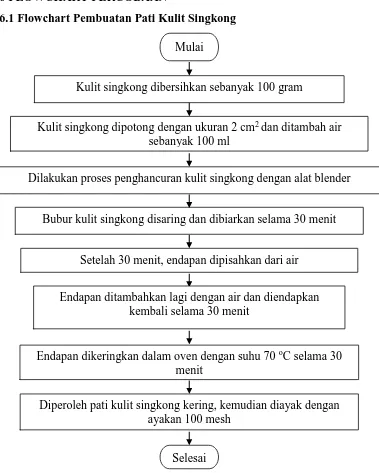
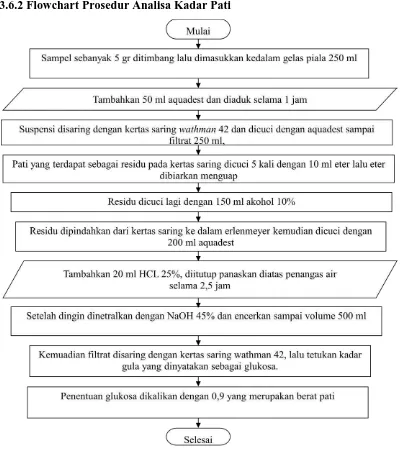
Pembuatan Bioplastik dari Pati Kulit Singkong (Manihot esculenta) Berpengisi Mikrokristalin Selulosa AvicelPH-101 (Wood pulp) dengan Plastisizer Sorbitol
Teks penuh
Gambar
Dokumen terkait
Hasil penelitian yang telah dilakukan menunjukkan bahwa pembuatan hidrogel dari pati kulit singkong dengan penambahan kitosan, sorbitol, dan natrium tripoliposfat
Anita et al (2013) menyatakan bahwa nilai kuat tarik dan persen perpanjangan saat putus bioplastik dari pati kulit singkong dengan penambahan pati lebih dari 5
Gambar D.5 Hasil FTIR Produk Lateks Karet Alam Dengan Penambahan Pengisi Selulosa Mikrokristalin dan Tanpa Penyerasi Alkanolamida. D.6 HASIL FTIR PRODUK LATEKS KARET ALAM
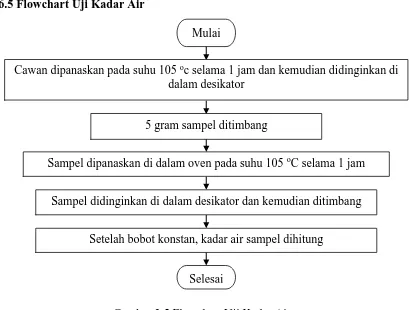
1. Mengetahui karakteristik pati talas meliputi kadar pati, kadar air, kadar abu, kadar amilosa, kadar amilopektin, kadar protein, kadar lemak dan profil gelatinisasi pati
Berdasarkan hasil analisis dengan menggunakan FTIR, maka gugus fungsi yang terdapat pada membrane dari kulit singkong memiliki gugus fungsi yang sama pada
Pada penelitian ini dilakukan untuk menguji efek penambahan gliserol dan sorbitol terhadap pati biji salak dan singkong sebagai bahan baku bioplastik ramah lingkungan,
Bioplastik dari pati kulit singkong khitosan dapat terdegradasi dengan bantuan EM 4 selama 10 hari, sehingga bioplastik pati kulit singkong khitosan adalah
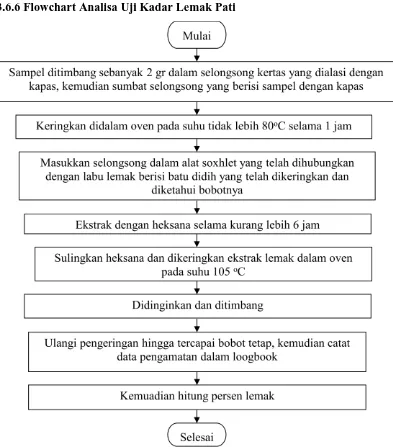
Hal ini dikarenakan pada bahan baku tepung ampas susu kedelai memiliki kadar lemak yang lebih tinggi dari pati singkong dan tepung terigu yaitu sebesar 1,82%.. Sehingga semakin banyak